
Sisu
Kopsude adenokartsinoom on mitteväikerakk-kopsuvähi (NSCLC) vorm, mis on kõige levinum kopsuvähk. NSCLC-d moodustavad 80% kopsu pahaloomulistest kasvajatest ja neist umbes 50% on adenokartsinoomid. Tänapäeval on adenokartsinoom kõige levinum kopsuvähi vorm naistel, asiaatidel ja alla 45-aastastel inimestel ning võib mõjutada isegi mittesuitsetajaid, kes pole kunagi ühtegi sigaretti suitsetanud.Ehkki adenokartsinoomi määr on meestel vähenenud ja naistel ühtlustunud, kasvab noorte mittesuitsetavate naiste arv jätkuvalt ning teadlased pole täiesti kindlad, miks. Üldiselt arvatakse, et geneetika, passiivne suitsetamine ja kokkupuude radooniga kodus on kõik soodustavad tegurid. Kahjuks puudub võimalike põhjuste uurimine, mis on osaliselt tingitud asjaolust, et kopsuvähki peetakse suures osas "suitsetaja haiguseks".
Miks kopsuvähk suureneb kunagi suitsetajatel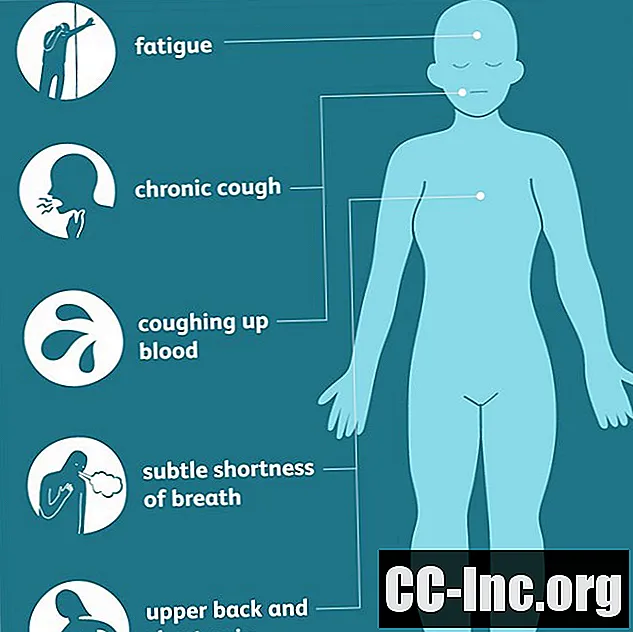
Kopsude adenokartsinoomi sümptomid
Kopsude adenokartsinoomid algavad tavaliselt kopsude välimise osa lähedal asuvatest kudedest ja võivad enne sümptomite ilmnemist olla seal pikka aega. Kui need lõpuks ilmuvad, on märgid sageli vähem ilmsed kui muud kopsuvähi vormid, avaldudes kroonilise köha ja verise röga alles haiguse hilisemates, kaugelearenenud staadiumides.
Seetõttu võivad mõned üldisemad varajased sümptomid (nagu väsimus, peen õhupuudus või ülaselja- ja rinnavalu) vahele jääda või olla seotud muude põhjustega. Seetõttu on diagnoosimine sageli hilinenud, eriti noorte ja mittesuitsetajate seas, kes ei pruugi vähki kunagi võimaluseks või ohuks pidanud.
Kopsuvähi sümptomid mittesuitsetajatelPõhjused
Nagu kõigi vähivormide puhul, on ka kopsu adenokartsinoomi põhjus suures osas teadmata. Uuringud pakuvad tungivalt, et geneetilised, keskkonnaalased ja elustiili tegurid mängivad rolli haiguse tekkes, ohus ja raskusastmes.
Geneetika
Ühena kolmest NSCLC alamtüübist arvatakse kopsu adenokartsinoomi seostavat teatud geneetiliste mutatsioonidega, mis võivad inimest eelsoodumuseks sellele haigusele.
Nende hulka kuulub epidermise kasvufaktori retseptori (EGFR) geeni mutatsioon, mis annab kehale juhised struktuurvalkude valmistamiseks ja reguleerib selle toimumise kiirust. On teada vähemalt 10 mutatsiooni, mis võivad mõjutada geeni ja põhjustada rakkude ebaharilikku paljunemist ja kontrolli alt väljumist.
EGFR-i mutatsioonid on sagedamini seotud vähem agressiivsete madala kuni keskmise astme adenokartsinoomidega.
Muud kopsu adenokartsinoomiga seotud mutatsioonid hõlmavad neid, mis mõjutavad Kirsteni roti sarkoomi (KRAS) geeni. Nagu EGFR, reguleerib KRAS ka rakkude kasvu, küpsemist ja surma; mutatsioone esineb 20–40% kopsu adenokartsinoomi juhtudest.
Inimestel, kelle kasvajatel on KRAS-mutatsioonid, on prognoos tavaliselt kehv. Isegi kui vähk reageerib algsele keemiaravile hästi, taastub haigus peaaegu alati.
Adenokartsinoomiga seotud mutatsioonid kanduvad mõnikord vanemalt lapsele. 2017. aasta ülevaade ajakirjas Onkoloogilised kirjad soovitab, et kopsuvähiga vanema või õe-venna olemasolu suurendab teie haiguse riski 50% võrra võrreldes inimestega, kellel pole perekonna ajalugu.
Muud mutatsioonid võivad esineda spontaanselt; teadlased pole kindlad, miks.
Tervisemured ja elustiil
Geneetikal on ainult osa kopsu adenokartsinoomi riskist. Teised tegurid aitavad märkimisväärselt kaasa, sealhulgas tubakasuitsutamine.
Kauaaegse õdede terviseuuringu kohaselt haigestuvad 30–40 aastat suitsetanud inimesed enam kui kaks korda sagedamini kopsu adenokartsinoomi kui need, kes kunagi ei suitsetanud. Risk kahekordistub veelgi, kui suitsetate rohkem kui 40 aastat.
Kasutatud suitsetamine suurendab ka teie riski.
Muud tegurid, mis seavad teid kopsu adenokartsinoomi ohtu, on järgmised:
- Õhusaaste, sealhulgas tahma ja heitgaasid
- Radooni kokkupuude kodus
- Tööalane kokkupuude kantserogeenidega nagu asbest või arseen
- Anamneesis kopsuhaigus, sealhulgas krooniline obstruktiivne kopsuhaigus (KOK) ja raske tuberkuloos (TB)
Need ja muud mittesuitsetamisega seotud riskitegurid on põhjuseks, miks 20% kopsuvähist esineb inimestel, kes pole elu jooksul sigaretti suitsetanud.
Mitteväikerakk-kopsuvähi põhjused ja riskifaktoridDiagnoos
Kopsuvähk tuvastatakse sageli esmakordselt, kui röntgenpildil nähakse kõrvalekaldeid, tavaliselt halvasti määratletud varju kujul. Kuigi see on ahastav, pakub leid vähemalt võimalust varajase diagnoosi saamiseks.
Koguni 25% kopsuvähi juhtudest ei tuvasta rinna röntgenülesvõte ühtegi ebakorrapärasust ja tagastab täiesti "normaalse" diagnoosi.
Vähktõve kahtluse korral võib kasutada muud, tundlikumat diagnostikat, sealhulgas:
- Kompuutertomograafia (kompuutertomograafia), rindkere skaneerimine, mis suudab tuvastada palju väiksemaid kõrvalekaldeid kui rindkere röntgen
- Magnetresonantstomograafia (MRI), mis kasutab piltide renderdamiseks magnetvälju
- Bronhoskoopia, protseduur, mille käigus sisestatakse kurgus paindlik ulatus kopsude suurte hingamisteede visuaalseks uurimiseks
- Positronemissioontomograafia (PET-skaneerimine), mis suudab visualiseerida metaboolse hüperaktiivsuse piirkondi (näiteks võib juhtuda vähirakkudega)
Kui pärast rindkere röntgenpildistamist on püsivaid probleeme, tuleks sellised lisauuringud tellida.
Võib kasutada ka röga tsütoloogiat, mille käigus hinnatakse köhitud sülje ja lima proovi, kuid seda peetakse varase vähi diagnoosimisel vähem kasulikuks.
Sõltuvalt tulemustest võib teie arst soovida diagnoosi kinnitamiseks saada kopsukoe proovi. Lisaks invasiivsematele kopsukoe biopsiatele võib uuem vereanalüüs, mida nimetatakse vedelaks biopsiaks, jälgida kopsuvähi rakkude spetsiifilisi geneetilisi kõrvalekaldeid, näiteks EGFR-i mutatsioone.
Kuidas diagnoositakse mitte-väikerakulist kopsuvähkiGeneetiline profileerimine
Üks põnevamaid edusamme onkoloogias on olnud geneetiliste testide kasutamine vähirakkude profileerimiseks. Nii toimides saavad arstid valida ravimeetodid, mis on suunatud nendele spetsiifilistele geneetilistele variatsioonidele.
Praegused juhised soovitavad kõigil kaugelearenenud kopsu adenokartsinoomiga isikutel läbi viia PD-L1 immunohistokeemia (PH-L1 IHC). See geneetiline test kirjeldab inimese vähki ja aitab ennustada ühe neljast haiguse raviks heaks kiidetud immunoteraapia ravimi potentsiaalset efektiivsust.
See tähendab, et PD-L1 testimine pole kaugeltki täiuslik ennustamaks, kes neile ravimitele reageerib või mitte. Muud testid, näiteks kasvaja mutatsioonikoormus (kasvajas esinevate mutatsioonide arv), võivad aidata kindlaks teha, kellele need uuemad sihipärased ravimeetodid kõige rohkem kasu saavad.
Oma molekulaarsete ja PD-L1 testide ülevaatamine on üks olulisemaid samme, kui esmakordselt diagnoositakse kaugelearenenud kopsu adenokartsinoom. Spetsiifilised ravimeetodid on saadaval mitte ainult EGFR-mutatsioonidega, vaid ka teiste ravitavate mutatsioonidega, nagu BRAF, ERBB2, ALK ümberkorraldused, ROS1 ümberkorraldused ja teised.
Ülevaade kopsuvähi geneetilisest testimisestVähi staadium
Kui vähidiagnoos on kinnitatud, määrab arst haiguse standardsete testide põhjal. Lavastuse eesmärk on teha kindlaks, kui kaugele arenenud kopsuvähk on ja kui suures ulatuses on see levinud (metastaasid).
Lavastamine aitab ravi suunata sobivamal viisil, nii et pahaloomulist kasvajat ei ravita liiga vähe (mõjutab tulemusi) ega ravita liiga palju (põhjustades tarbetuid kõrvaltoimeid).
Kui kaalutakse juhtumit varjatud kopsuvähk, see tähendab, et vähirakke leidub röga, kuid pildistamise uuringute abil ei õnnestu leida kopsukasvajat. 0. etapp tähendab, et vähk piirdub hingamisteede vooderdisega ja ei ole veel invasiivne.
Peale selle on neli etappi, mis on määratletud järgmiselt. Neid termineid kasutatakse ravivõimaluste arutamisel.
| Klassifikatsioon | Vastav (ad) etapp (id) | Ravivõimalused |
|---|---|---|
| Varases staadiumis kopsuvähk | • 1. etapp: lokaliseeritud ja ei levinud lümfisõlmedesse • 2. etapp: levib lümfisõlmedesse, kopsude vooderdisse või nende peamistesse kanalitesse | Operatsiooniga potentsiaalselt ravitav |
| Lokaalselt kaugele arenenud kopsuvähk | 3A etapp: levib kasvajaga samal kehapoolel asuvate lümfisõlmedeni, kuid mitte kaugetesse piirkondadesse | Operatsioon võimalik; tavaliselt on vajalik adjuvantravi keemiaravi ja kiiritusraviga |
| Kaugelearenenud kopsuvähk | • 3B etapp: levib kaugetesse lümfisõlmedesse või tungib rindkere teistesse struktuuridesse • 4. etapp: levige teise kopsu, teise kehapiirkonna või kopsu või südant ümbritseva vedeliku hulka | Parim on mittekirurgiline ravi. Kõiki harva esinevaid juhtumeid, välja arvatud mõned, peetakse töövõimetuks. |
Ülevaade kopsuvähi staadiumitestRavi
Sõltuvalt haiguse staadiumist võib ravi hõlmata ühte ravi või kombinatsiooni.
- Kirurgia võib varases staadiumis pakkuda kas üksi või koos kemoteraapia ja / või kiiritusraviga. Eduka operatsiooni korral on operatsioonil kopsuvähi ravimiseks parimad võimalused.
- Keemiaravi võib kasutada üksi, koos kiiritusraviga või enne või pärast operatsiooni.
- Suunatud ravimeetodid rünnata konkreetseid geneetilisi mutatsioone, tuvastades vähirakkudel spetsiifilised valgud ja blokeerides nende paljunemisvõime. Võimaluste hulka kuuluvad Tarceva (erlotiniib), Iressa (gefitiniib), Gilotrif (afatiniib), Xalkori (krisotiniib), Zykadia (tseritiniib), Alecnensa (alektiniib) ja Tagrisso (osimertiniib). Veel tehakse kliinilisi uuringuid.
- Kiiritusravi võib kasutada kas vähi raviks või metastaatilise vähiga patsientide tõrjeks. Väiksemate vähkide korral, kuhu kirurgia ei jõua, võib kasutada rohkem suunatud radiatsioonivorme (stereotaktiline keha kiiritusravi (SBRT), prootonravi). SBRT-d kasutatakse nüüd ka aju metastaaside ja muude metastaaside raviks kopsuvähki põdevatel inimestel, kui esineb vaid väheseid.
- Immuunravi eesmärk on rakendada organismi immuunsüsteemi vähiga võitlemiseks. Praeguste võimaluste hulka kuuluvad Opdivo (nivolumab), Keytruda (pembrolizumab), Tecentriq (atezolizumab) ja Imfinzi (durvalumab) 3. ja 4. astme kopsuvähi korral.
Sihtotstarbelised ravimeetodid on palju vähem üldistatud kui varasema põlvkonna ravimeetodid, mis ründasid nii terveid kui ka ebatervislikke rakke, mille tulemuseks olid rasked ja isegi talumatud kõrvaltoimed. Kliiniliste uuringute käigus tuvastatakse levinumad mutatsioonid, mida saab ravimitega sihtida. See ravivaldkond on alles lapsekingades ja kiiresti arenev.
Sihtotstarbeliste ja muude ravimeetodite kliinilised uuringud pakuvad lootust neile, kelle heakskiidetud ravi on kas ebaõnnestunud või põhjustab tõsiseid kõrvaltoimeid. NCI soovitab kopsuvähiga inimestel kaaluda kliinilises uuringus osalemist.
Varem oli tõenäosus, et kliiniline uuring muudab vähihaige inimese jaoks midagi väikest, kuid see muutub kiiresti, kui tuvastatakse vähirakkude jagunemise raja spetsiifilised sihtmärgid. Paljud inimesed, kellel on 4. astme kopsuvähk, on elus ainult nende osalemise tõttu kliinilises uuringus.
Lõpuks soovitavad paljud arstid saada teise arvamuse mõnelt teiselt spetsialistilt või ühelt riikliku vähiinstituudi (NCI) määratud ravikeskusest, kes aktiivselt osalevad kopsuvähi uuringutes. See võib aidata teil saada kõige ajakohasemat teavet ravi kohta ja paremini teha teadlikke valikuid.
Kuidas ravitakse mitte-väikerakulist kopsuvähkiSõna Verywellist
Kuna kopsuvähi varajasi sümptomeid on sageli raske märgata, on keskmine viie aasta elulemus vaid umbes 18%. Varases staadiumis diagnoositud inimeste jaoks on väljavaade palju paljutõotavam.
See toob esile vajaduse suurema teadlikkuse järele kopsuvähi mittespetsiifiliste või ebatüüpiliste sümptomite suhtes. Sümptomid võivad iseenesest olla lihtsad. Koos võivad nad heisata punase lipu, mis võib viia varase diagnoosimise ja varasema, tõhusama ravini.
10 parimat vähihaiglat USA-s